Что создаём?
Графитовый анодный материал
В литий-ионных аккумуляторах графит используется в качестве анодного материала благодаря способности интеркалировать (встраивать) ионы лития между своими слоями в процессе зарядки. Это обеспечивает высокую электронную проводимость, стабильность при многократных циклах заряда-разряда и достаточную ёмкость для накопления энергии. Несмотря на поиск более эффективных альтернатив, графит остаётся ключевым материалом для анодов из-за доступности и отработанной технологии применения.
Вот почему графит так важен:
-
Хранение ионов лития
Графит имеет слоистую структуру, между которыми могут внедряться (интеркалироваться) ионы лития (Li⁺) во время зарядки. Это похоже на "впитывание" лития в графитовые слои без разрушения материала.
-
Стабильность и долговечность
- Графит химически инертен в рабочем диапазоне напряжений
- Минимально расширяется/сжимается (всего на ~10%)
-
Проводимость
Графит хорошо проводит электроны, что важно для эффективного переноса заряда во внешней цепи.
-
Безопасность
В отличие от чистого лития, графит предотвращает образование дендритов (опасных игольчатых наростов), которые могут пробить сепаратор и вызвать КЗ.
-
Дешевизна и доступность
Графит — относительно недорогой материал по сравнению с альтернативами (например, кремнием).
Из чего?
Графит
Графит — это аллотропная модификация углерода, обладающая гексагональной слоистой кристаллической структурой. Каждый слой состоит из шестиугольных ячеек с прочными ковалентными связями между атомами, слабые ван-дер-ваальсовы взаимодействия между слоями обеспечивают его мягкость, электропроводность и способность к расслоению.
Уникальность графита — в сочетании свойств: электропроводность, термостойкость, химическая инертность и способность к расслоению. Это делает его универсальным материалом, замену которому в большинстве сфер пока не нашли.
Его свойства делают его незаменимым в различных отраслях:
- Металлургия и производство
- Электротехника и энергетика
- Машиностроение
- Химическая промышленность
- Авиакосмическая отрасль
Высокая термостойкость (до 3000°C) позволяет использовать графит в огнеупорных материалах (тигли, формы для литья), а также в электродах дуговых печей.
Проводит электричество благодаря подвижным электронам в слоях. Применяется в анодах литий-ионных аккумуляторов, токосъёмниках, компонентах электродвигателей.
Служит сухой смазкой для высокотемпературных механизмов (например, в двигателях или подшипниках), так как слои легко скользят друг относительно друга.
Устойчив к агрессивным средам. Используется в уплотнителях, теплообменниках, реакторах для работы с кислотами и щелочами.
Лёгкость и прочность графитовых материалов делают их идеальными для деталей ракет, спутников и самолётов.
Для чего?
Литий-ионный аккумулятор
Литий-ионные аккумуляторы — технологический стандарт XXI века, объединяющий эффективность, универсальность и экологичность. Их развитие продолжает стимулировать переход к устойчивой энергетике и электротранспорту.
Преимущества
- Высокая энергетическая плотность — хранят больше энергии на единицу массы, чем другие типы аккумуляторов, что делает их компактными и легкими.
- Низкий саморазряд — теряют всего 1–5% заряда в месяц, сохраняя энергию дольше.
- Долгий срок службы — выдерживают 500–1500 циклов заряда-разряда до снижения ёмкости на 20%.
- Быстрая зарядка — адаптируются к высоким токам без значительного ущерба для структуры.
- Экологичность — не содержат токсичных тяжёлых металлов (например, свинца или кадмия).
Литий-ионные аккумуляторы стали основой технологического прогресса:
- Портативная электроника — питают смартфоны, ноутбуки, планшеты.
- Электромобили — обеспечивают высокий запас хода (Tesla, Nissan Leaf, BYD,..).
- Зелёная энергетика — накапливают энергию от солнечных панелей и ветрогенераторов.
- Медицина — используются в имплантах и портативных устройствах.
Их массовое применение сокращает зависимость от ископаемого топлива и снижает выбросы CO₂.
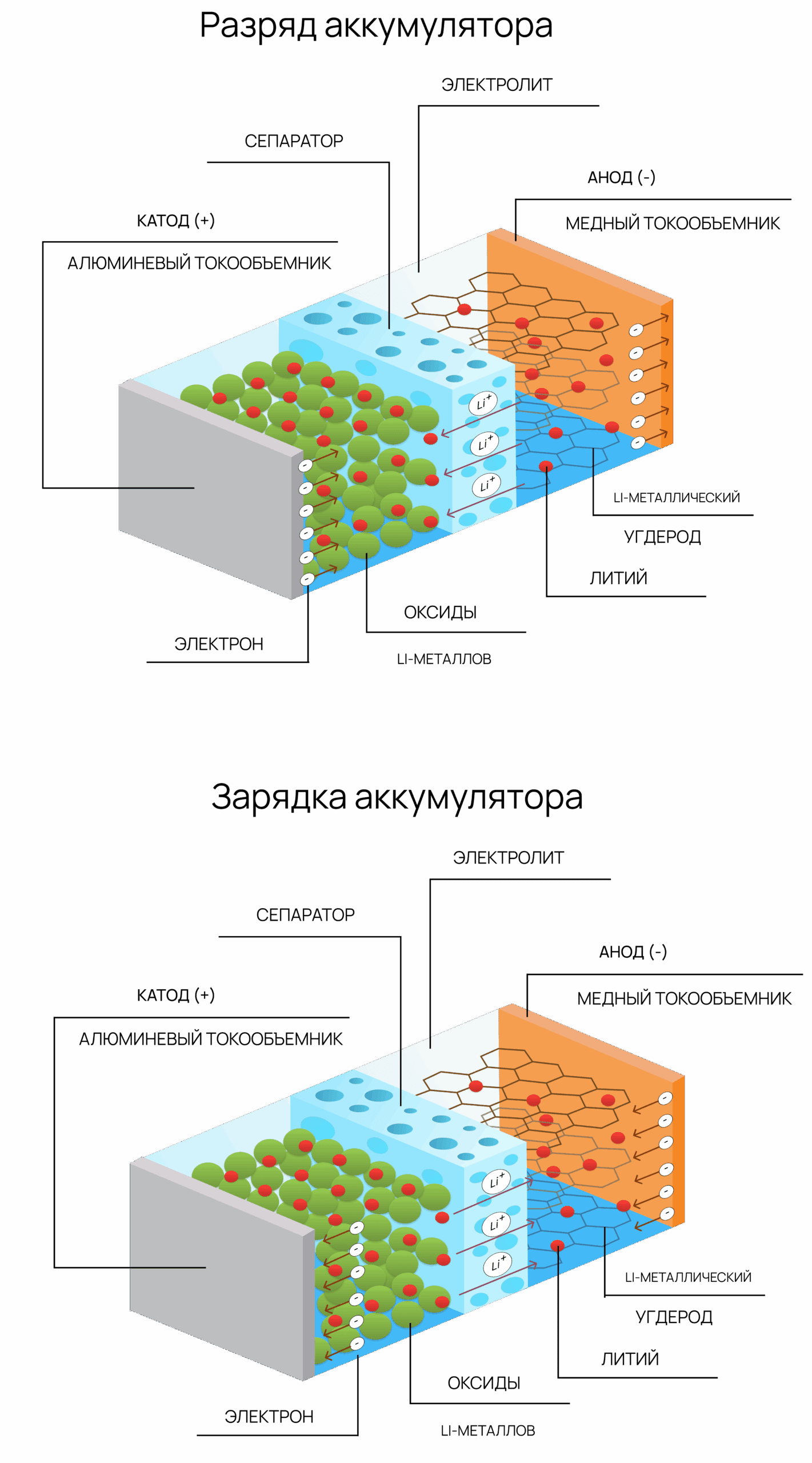
Принцип работы литий-ионного аккумулятора (Li-ion):
- Основные компоненты:
- Анод (обычно графит) — отдаёт ионы лития при разряде.
- Катод (оксид металла, например, LiCoO₂) — принимает ионы.
- Электролит (соль лития в органическом растворителе) — проводит ионы Li⁺.
- Сепаратор — разделяет электроды, предотвращая короткое замыкание.
- Разрядка (работа):
- Ионы Li⁺ перемещаются от анода к катоду через электролит.
- Электроны движутся по внешней цепи (питание устройства), создавая ток.
- Зарядка:
- Внешний ток "заталкивает" ионы Li⁺ обратно на анод.
- Электроны возвращаются через цепь заряда.